Перечень лекарственных средств, лишённых регистрации и отозванных из оборота в ноябре
В ноябре 2025 года по решению производителей из гражданского оборота было отозвано 44 серии лекарственных препаратов. Обращение ещё 20 серий было прекращено Росздравнадзором из‑за обнаруженных несоответствий отобранных образцов требованиям нормативной документации. Кроме того, появилась информация об отзыве сертификатов пригодности на шесть фармсубстанций.
Мы собрали всю важную официальную информацию из писем Росздравнадзора в одной статье: списки отозванных препаратов, причины отзыва и краткие инструкции, как действовать в случае обнаружения их в ассортименте аптеки.
Отзыв
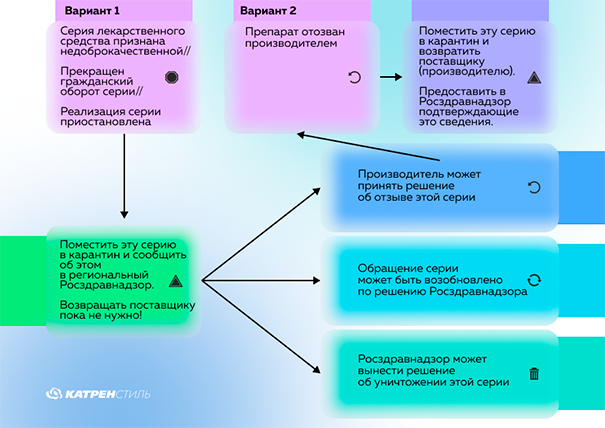
Отзыв препаратов происходит по инициативе производителя или его представителя (в случае с импортными ЛС), а Росздравнадзор информирует об этом всех участников процесса обращения ЛС и рекомендует им, как поступить. Рекомендации при отзыве ЛП стандартные.
Что делать производителю?
Предоставить в Росздравнадзор сведения об изъятии из обращения указанной серии лекарственного препарата.
Что делать аптекам и другим субъектам обращения ЛС?
Предоставить в территориальный орган Росздравнадзора сведения, подтверждающие возврат указанной серии лекарственного препарата поставщикам (производителю).
Мы объединили отзываемые препараты в одной таблице. В качестве причины в письмах Росздравнадзора зачастую указано «несоответствие качества препарата требованиям нормативной документации» по тому или иному показателю.
Таблица 1. Отозванные препараты
| Препарат | Серия | Производитель | Несоответствие показателю |
| «Мебетан, капсулы с пролонгированным высвобождением, 200 мг, 10 шт., упаковки ячейковые контурные (3), пачки картонные» | 0101123, 0111123 | ООО «Фарма Капитал» (Россия) | «Растворение» |
| «Бетагистин, таблетки, 24 мг, 10 шт., упаковки ячейковые контурные (6), пачки картонные» | 1651224 | ООО «Пранафарм» (Россия) | «Родственные примеси» |
| «Эналаприл, таблетки, 10 мг, 10 шт., упаковки ячейковые контурные (2), пачки картонные» | 611023 | ООО «Пранафарм» (Россия) | «Родственные примеси» |
| «Бисопролол-прана, таблетки, покрытые плёночной оболочкой, 2,5 мг, 10 шт., упаковки ячейковые контурные (4), пачки картонные» | 100225 | ООО «Пранафарм» (Россия) | «Описание» |
| «Глюконорм, таблетки покрытые плёночной оболочкой, 2,5 мг + 400 мг, 20 шт., блистеры (2), пачки картонные» | T2G010323, T2G020323, T2G030323, T2G040323, T2G050323, T2G060323, T2G070323, T2G130523, T2G080423, T2G090423, T2G100423, T2G110423, T2G120423, T2G140523, T2G150623, T2G160623, T2G170623, T2G180623, T2G190823, T2G200823, T2G210823, T2G220823, T2G230823, T2G240823, T2G010224, T2G070324, T2G020224, T2G030224, T2G040224, T2G050224, T2G060224, T2G080324, T2G090324, T2G100324, T2G130424, T2G140424, T2G150424, T2G160424, T2G170624 | ОАО «Фармстандарт-Томскхимфарм» (Россия) | В связи с выявлением несоответствия герметичности первичной упаковки (блистеры), которое обнаружено при изучении стабильности данных серий лекарственного препарата |
Прекращение обращения
Следующая группа — это ЛС, оборот которых прекращён по инициативе Росздравнадзора после обнаружения в ходе проверок несоответствия серий препаратов нормативным требованиям.
Что делать аптекам?
Провести проверку наличия указанных серий лекарственных препаратов и, в случае обнаружения таких ЛС, поместить их в карантин. О результатах проверки нужно проинформировать территориальные органы Росздравнадзора.
Таблица 2. Лекарственные средства, оборот которых приостановлен Росздравнадзором
| Препарат | Серия | Производитель | Несоответствие показателю |
| «Левофлоксацин, таблетки, покрытые плёночной оболочкой, 500 мг, 10 шт., упаковки ячейковые контурные (1), пачки картонные» | 081124 | ООО «Интерфарма» (Россия) | «Описание» |
| «Икативиз, раствор для подкожного введения, 10 мг/мл, 3 мл, шприцы, пачки картонные /в комплекте с иглой» | 10124 | АО «Фармасинтез» (Россия) | «Осмоляльность» |
| «Каптоприл, таблетки, 0,05 г, 10 шт., упаковки ячейковые контурные (4), пачки картонные» | 1191123, 391224 | ООО «Пранафарм» (Россия) | «Родственные примеси» |
| «Цитрамон П, таблетки, 10 шт., упаковки ячейковые контурные (2), пачки картонные» | 290822 | ОАО «Дальхимфарм» (Россия) | «Описание», «Растворение», «Родственные примеси (салициловая кислота)», «Однородность дозирования (ацетилсалициловая кислота)», «Количественное определение» |
| «Левофлоксацин, таблетки, покрытые плёночной оболочкой, 500 мг, 10 шт., упаковки ячейковые контурные (1), пачки картонные» | 111124 | ООО «Интерфарма» (Россия) | «Растворение» |
| «Меновазин, раствор для наружного применения спиртовой, 40 мл, флаконы (1), пачки картонные» | 400225 | АО «Флора Кавказа» (Россия) | «Описание», «Объём содержимого упаковки», «Маркировка» |
| «Бетагистин, таблетки, 16 мг, 10 шт., упаковки ячейковые контурные (3), пачки картонные» | 181224 | ООО «Пранафарм» (Россия) | «Родственные примеси» |
| «Цефтриаксон, порошок для приготовления раствора для внутривенного и внутримышечного введения 1 г, флаконы (50), коробки картонные, для стационаров» | 580524 | АО «Биохимик» (Россия) | «Бактериальные эндотоксины» |
| «Бетагистин, таблетки, 24 мг, 10 шт., упаковки ячейковые контурные (6), пачки картонные» | 1651224 | ООО «Пранафарм» (Россия) | «Родственные примеси» |
| «Иринова, концентрат для приготовления раствора для инфузий, 20 мг/мл, 11,5 мл, флаконы (1), пачки картонные» | 60823 | АО «Фармасинтез-Норд» (Россия) | «Механические включения. Видимые частицы», «Примеси» |
| «Иринова, концентрат для приготовления раствора для инфузий, 20 мг/мл, 5 мл, флаконы (1), пачки картонные» | 20624А | АО «Фармасинтез-Норд» (Россия) | «Механические включения. Видимые частицы» |
| «Иринова, концентрат для приготовления раствора для инфузий, 20 мг/мл, 2 мл, флаконы (1), пачки картонные» | 80923В | АО «Фармасинтез-Норд» (Россия) | «Механические включения. Видимые частицы», «Прозрачность», «Описание» |
| «Иринова, концентрат для приготовления раствора для инфузий, 20 мг/мл, 2 мл, флаконы (1), пачки картонные» | 91123А | АО «Фармасинтез-Норд» (Россия) | «Описание» |
| «Амизолид, таблетки, покрытые плёночной оболочкой, 600 мг, 10 шт., упаковки ячейковые контурные, пачки картонные» | 20323 | АО «Фармасинтез» (Россия) | «Растворение» |
| «Ацетилсалициловая кислота Кардио, таблетки кишечнорастворимые, покрытые плёночной оболочкой, 100 мг, 15 шт., упаковки ячейковые контурные (8), пачки картонные» | 10323 | АО «ПФК Обновление» (Россия) | «Растворение» |
| «Кальция глюконат, таблетки, 500 мг, 10 шт., упаковки ячейковые контурные (2), пачки картонные» | 20224 | ОАО «Уралбиофарм» (Россия) | «Маркировка» (на вторичной упаковке в адресе производителя название города указано в редакции: «ЕКАТИРИНБУРГ») |
| «Уголь активированный Авексима, таблетки, 250 мг, 10 шт., упаковки ячейковые контурные (5), пачки картонные» | 150824 | ООО «Авексима Сибирь» (Россия) | «Однородность массы» |
| «Амлодипин- АКОС, таблетки, 10 мг, 15 шт., упаковки ячейковые контурные (4), пачки картонные» | 691224, 701224 | ПАО «Синтез» (Россия | «Маркировка» нормативного документа по качеству (на первичной упаковке дополнительно указано: «г. Курган») |
Кроме того, в ноябре были сняты с посерийного контроля серии 30325, 40325, 50425 лекарства «Вазелиновое масло, масло для приёма внутрь, 100 мл, флаконы (1), пачки картонные» производства АО «Флора Кавказа» (Россия) на основании протоколов испытаний ФГБУ «ИМЦЭУАОСМП» Росздравнадзора (Ставропольский филиал).
На посерийный выборочный контроль переведены:
- с 02 декабря 2025 года — препарат «Каптоприл, таблетки 0,05 г, 10 шт, упаковки ячейковые контурные (4), пачки картонные» производства ООО «Пранафарм» (Россия);
- с 19 ноября 2025 года — лекарственное средство «Амлодипин-АКОС, таблетки, 10 мг, 15 шт., упаковки ячейковые контурные (4), пачки картонные» производства ПАО «Синтез» (Россия);
- с 17 ноября 2025 года — лекарство «Амизолид, таблетки, покрытые плёночной оболочкой, 600 мг, 10 шт., упаковки ячейковые контурные (1), пачки картонные» производства АО «Фармасинтез» (Россия);
- с 17 ноября 2025 года — лекарственное средство «Иринова, концентрат для приготовления раствора для инфузий, 20 мг/мл, 2 мл, флаконы (1), пачки картонные» производства АО «Фармасинтез-Норд» (Россия).
Также Росздравнадзор сообщил о приостановлении сертификата пригодности на субстанцию СЕР 2019–020 Меклозина дигидрохлорид производства компании «THINQ PHARMA-CRO LIMITED» (Thane, Индия). Решение принято в связи с невозможностью компании предоставить запрошенную информацию о ходе процедуры продления.
Кроме того, ведомство опубликовало письма об отзыве сертификатов пригодности на:
- субстанции CEP 2010–200 и СЕР 2008–133 «Желатин» производства компании «QINGHAI GELATIN COMPANY LIMITED» (No. 18 Weiyi Road Biological Estate Garden of Qinghai, 810 016 Xining, Qinghai Province, China) в связи с прекращением деятельности компании и нежелании поддерживать свои СЕР;
- субстанцию СЕР 2004–155 «Тригидрат рутозида (Rutoside trihydrate)» производства компании «Quercegen Pharmaceuticals LLC» (Норт-роуд Сьют, 144, Садбери, 2100, Соединённые Штаты Америки) в связи с прекращением деятельности указанной компании;
- субстанции СЕР 1996–106 «Глицерофосфат кальция», СЕР 1999–164 «Гидрат глюконата железа», СЕР 2012–221 «Глюконат цинка» производства «Givaudan-Lavirotte (Живодан-Лавиротт) 56 Rue Paul Cazeneuve (Улица Поля Казнева, 56) France-69008 Lyon (Лион, Франция-69008)» в связи с прекращением всех операций и существования компании.
Следите за оперативными сообщениями о прекращении импорта или производства лекарственных препаратов (и об изменениях в инструкциях и новых данных по безопасности применения ЛС) в разделе «Новости», а также не пропускайте наш следующий ежемесячный обзор с перечислением всех изъятых и отозванных из обращения серий ЛС.
